X
Звонки для Украины
Звонки для Европы
Звонки для США

Грибок, населяющий древние захоронения, может стать союзником в борьбе с лейкозом
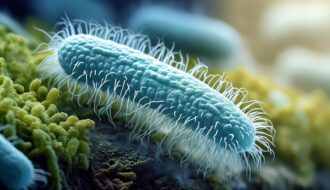
Исследователи обнаружили, что молекулы, полученные из ядовитого грибка Aspergillus flavus, который часто встречается в древних захоронениях, оказывают мощное противораковое воздействие. В ходе экспериментов с клетками лейкоза эти соединения показали эффективность, сопоставимую с препаратами, одобренными Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA). Результаты исследования открывают новые горизонты в разработке противораковых лекарств на основе грибковых соединений.
Aspergillus flavus — это ядовитая плесень с желтыми спорами, известная своей опасностью для здоровья. Она выделяет токсины, которые могут вызывать смертельные инфекции легких, особенно у людей со слабым иммунитетом или хроническими заболеваниями. Грибок встречается повсюду: его можно найти в почве, перегнивающих органических веществах, погребах, гробницах, а также в плохо хранящихся злаках и сухофруктах.
Популярность Aspergillus flavus приобрел после загадочных смертей нескольких археологов, принимавших участие в раскопках гробницы Тутанхамона в 1920-х годах. Это породило слухи о «проклятии фараона», однако впоследствии врачи предположили, что причиной гибели людей стала инфекция, вызванная спорами грибка, которые хранились в гробнице тысячелетиями.
Кроме того, A. flavus мог быть связан со смертью 10 из 12 ученых, которые исследовали гробницу польского короля Казимира IV в 1970-х годах. Дальнейшие анализы подтвердили наличие большого количества спор этого грибка в захоронении.
Несмотря на свою опасность, многие грибы обладают ценными лечебными свойствами. В новом исследовании, опубликованном в журнале Nature Chemical Biology, ученые из Университета Пенсильвании показали, что A. flavus может стать неожиданным источником противораковых соединений. «Грибы подарили нам пенициллин, — говорит Шерри Гао, доцент Университета Пенсильвании и ведущий автор исследования. — Наши результаты показывают, что в природных соединениях еще много неизученного потенциала для создания лекарств».
Многообещающее действие против лейкоза
Исследователи выделили из грибка особый класс пептидов — рибосомально синтезированные и посттрансляционно модифицированные пептиды (RiPP). Их обнаружение является сложным, поскольку RiPP грибкового происхождения часто путают с нерибосомными пептидами.В то время как тысячи бактериальных RiPP уже известны, у грибов их найдено лишь несколько.
Команда Гао проанализировала 12 штаммов Aspergillus, чтобы выявить наиболее перспективные RiPP. Оказалось, что соединения, производимые A. flavus, обладают высокой биологической активностью. Эти пептиды кодируются специфическим белком, и его отключение полностью прекращало их выработку.
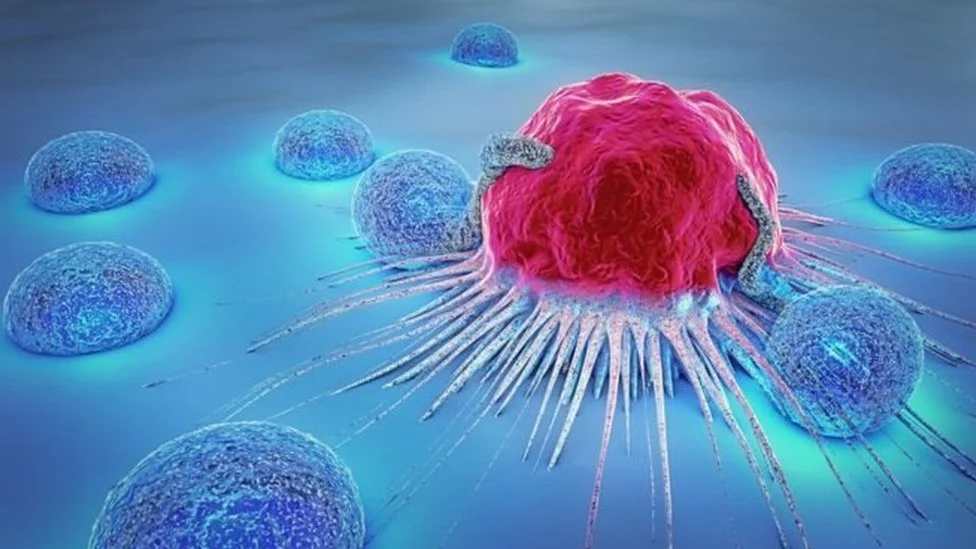
Ученые выделили четыре RiPP из A. flavus и обнаружили, что они имеют необычную структуру из вложенных колец. Новые молекулы, названные «асперигимицинами», продемонстрировали значительную противораковую активность. Две из них особенно эффективно подавляли клетки лейкоза.
Дальнейшие исследования показали, что асперигимицины нарушают процесс деления клеток, блокируя образование микротрубочек. Это объясняет их противораковое действие, поскольку раковые клетки характеризуются бесконтрольным размножением.
Эффективность на уровне одобренных препаратов
В другом эксперименте ученые добавили к RiPP липид — компонент маточного молочка, питательного вещества, которое пчелы производят для кормления личинок и матки. В результате комбинация показала эффективность, сравнимую с цитарабином и даунорубицином — препаратами, которые десятилетиями используются для лечения лейкоза.
Липиды помогли новым соединениям проникать в клетки. Чтобы понять механизм этого эффекта, исследователи выборочно активировали и деактивировали гены в раковых клетках. Оказалось, что ген SLC46A3 играет ключевую роль, регулируя проникновение асперигимицинов в клетки через лизосомы.
«Этот ген действует как шлюз, — объясняет Цююэ Ни, соавтор исследования. — Он не только облегчает попадание асперигимицина в клетки, но и может помочь другим циклическим пептидам, которые обычно требуют модификации для эффективного проникновения».
При этом асперигимицины почти не влияли на клетки рака груди, печени и легких, а также на бактерии и другие грибы. Это указывает на их избирательное действие.
Кроме того, ученые обнаружили похожие гены в других грибах, что свидетельствует о возможном существовании неизученных RiPP с терапевтическим потенциалом. Следующим шагом станет тестирование асперигимицинов на животных моделях, а в случае успеха — клинические испытания.
Категории:
Новости медицины
Все категории:
- Война (11)
- Заболевания (6)
- Интервью с докторами (22)
- Медицинские статьи (97)
- Новости медицины (334)
Появились вопросы?
Получите бесплатную консультацию от наших специалистов